cieczowa Ciecz-cia Cieczowa Ciecz-ciecz · 2020. 4. 19. · Chromatografia adsorpcyjna w normalnym...
Transcript of cieczowa Ciecz-cia Cieczowa Ciecz-ciecz · 2020. 4. 19. · Chromatografia adsorpcyjna w normalnym...


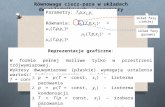
czoło kolumny
wypływ
1. chromatografia
kolumnowa
2. chromatografia
cienkowarstwowa
czoło
start
Ze względu na kształtu złoża można podzielić

Chromatografia
Gazowa
Gazowo-cieczowa
Gaz-ciało stałe
Cieczowa
Ciecz-ciało stałe
Ciecz-ciecz

– zdolna do oddziaływania ze składnikami mieszaniny matryca nie
przemieszczająca się w procesie chromatografii, zwykle ciekła lub stała
– ciecz lub gaz oddziałujący ze składnikami rozdzielanej mieszaniny,
przemieszczający się wzdłuż fazy stacjonarnej
– stała substancja wypełniająca kolumnę lub pokrywająca płytkę, może stanowićfazę stacjonarną lub „podporę” dla stacjonarnej fazy ciekłej
– ciekła faza ruchoma (zwłaszcza w chromatografii kolumnowej)
– wypływająca z kolumny faza ruchoma zawierająca rozfrakcjonowane składniki
mieszaniny
– faza stacjonarna o właściwościach adsorpcyjnych
- składnik mieszaniny ulegający adsorpcji
– obraz graficzny frakcji wypływających z kolumny chromatograficznej
– objętość, w której wypływa z kolumny dana frakcja
– czas, w którym wypływa ze standaryzowanej kolumny dana frakcja

Niezależnie od sposobu przeprowadzenia rozdziału- w chromatografii cienkowarstwowej
- w chromatografii kolumnowej,
są wykorzystywane te same mechanizmy
oddziaływań międzycząsteczkowych
Podział chromatografii ze względu na naturę zjawisk
będących podstawą procesu chromatograficznego
➢ Chromatografia adsorpcyjna
➢ Chromatografia podziałowa
➢ Chromatografia jonowymienna
➢ Chromatografia żelowa (wykluczenia, sitowa lub sączenie
molekularne)

• Chromatogram rozwijamy przemywając złoże (adsorbent w kolumnie)
rozpuszczalnikiem, czyli dzielimy mieszaninę na grupy związków i wymywamy
je (eluujemy) z kolumny, zbierając kolejne frakcje eluatu (rozpuszczalnika z
eluującymi się związkami).
• Oddziaływania międzycząsteczkowe powodują, że rozdzielane substancje w
niejednakowym stopniu zatrzymują się na adsorbencie. Im większe
powinowactwo analitu do fazy stacjonarnej, tym analit jest silniej przez niązatrzymywany.
• Analit z adsorbentu wymywany jest fazą ruchomą. Im silniej zatrzymywany
analit, tym później opuszcza kolumnę, ma większą retencję (opóźnienie w
stosunku do przepływu fazy ruchomej).
• Objętość fazy ruchomej potrzebna do wymycia analitu to objętość retencji,
a czas, w jakim analit zostaje wymyty z kolumny to - czas retencji.
• Objętość retencji i czas retencji analitu liczy się od momentu naniesienia na
kolumnę do momentu opuszczenia kolumny przez maksimum jego stężenia.

Etapy rozdziału chromatograficznego
Rozdziałna nośniku
Graficzne przedstawienie wyników
rozdziału chromatograficznego: profil elucji

1 - Przygotowanie i
pakowanie kolumny
2 - Złoże gotowe do
rozdziału
3 - Nakładanie
mieszaniny
4, 5 - Rozdział
6 - Zbieranie frakcji
1 2 3
4 5 6

Faza stacjonarna: ciało stałe,
Przykłady: żel krzemionkowy, ziemia okrzemkowa, węgiel aktywny,
tlenek glinu, skrobia, octan celulozy
Faza ruchoma (eluent): ciecz o odpowiedniej polarności
Mechanizm oddziaływania: powierzchniowa fizyczna adsorpcja
składników mieszaniny do złoża i ich wypłukiwanie
(adsorpcja/desorpcja)
Adsorpcja wielokrotna w czasie i selektywna
Właściwości warunkujące rozdział: różnica polarności składników
mieszaniny
Ustalenie warunków rozdziału: dopasowanie stopnia polarności
złoża/eluentu
Niewielkie ilości substancji, których rozdzielenie za pomocąkrystalizacji czy destylacji jest niemożliwe
Chemisorpcja: sorpcja powierzchniowa związana z silniejszymi
oddziaływaniami chemicznymi (np. jonowymiana)
Proces chromatograficzny to wielokrotna sorpcja i desorpcja substancji z fazy
ruchomej do stacjonarnej i odwrotnie, z fazy stacjonarnej do fazy ruchomej.

: woda>alkohol > acetonitryl >heksan
: żel krzemionkowy (tlenek krzemu) >węglowodory > węglowodory aromatyczne
: sole > kwasy > alkohole > ketony > etery > związki aromatyczne > związki alifatyczne długołańcuchowe
Sole Alkohole Etery Aromatyczne Fluorowane
Kwasy Ketony AlifatyczneHalogenowane
Węglowodory
Faza ruchomaWoda Alkohol Acetonitryl THF Heksan
www.waters.com/webassets
Faza stacjonarnaKrzemionka CN C2 C12(OOS)

Chromatografia adsorpcyjna w normalnym układzie faz wykorzystuje oddziaływania polarnych grup funkcyjnych rozdzielanych składników z polarnymi centrami aktywnymi obecnymi na powierzchni fazy stacjonarnej. Faza ruchoma jest niepolarna.
W układzie faz odwróconych (RP) faza stacjonarna jest niepolarna, a faza ruchoma polarna.

Zadanie: należy rozdzielić metodą chromatografii adsorpcyjnej z użyciem żelu krzemionkowego (faza nieruchoma) i alkoholu metylowego jako eluentu (faza ruchoma) mieszaninę dwóch barwników organicznych różniących się polarnością: A-bardziej polarny, i B-mniej polarny.
Który z barwników, A czy B, wypłynie z kolumny jako pierwszy, a który jako drugi?
Odpowiedź: Pierwszy wypłynie ……………. Drugi wypłynie …………….
Wytłumacz, dlaczego?

Szczególny typ chromatografii adsorpcyjnej,
chemisorpcja analitu związana
z oddziaływaniem jonowym
Faza stacjonarna: jonit (żywica jonowymienna);
Faza ruchoma: roztwór
buforowy o określonym pH,
zdolny do zmiany jonizacji
analitu
Zasada rozdziału: różnice
w ładunku powierzchniowym
skladników mieszaniny
www.waters.com/webassets

❑Wymieniacz jonowy jest substancją, która w zetknięciu z roztworem
wymienia część swoich jonów na jony z roztworu.
❑W jego strukturze można wyróżnić nierozpuszczalną matrycępołączoną wiązaniami kowalencyjnymi z określonymi grupami
funkcyjnymi, które ulegają jonizacji i mogą w sposób odwracalny
asocjować z jonami przeciwnego znaku, tzw. przeciwjonami.
❑ Kationy i aniony będące jonami wymiany, czyli tzw. przeciwjony,
pochodzą z roztworu buforowego używanego do równoważenia
złoża. Podczas rozdziału chromatograficznego przeciwjony sązastępowane przez obdarzone odpowiednim ładunkiem
cząsteczki białka.

Po
wie
rzch
nio
wy ład
un
ek c
ząste
czki
/ b
iałk
a
Ładunek białka
w pH > pIWymiana anionu
0 14
+
Ładunek białka
w pH < pI
Wymiana kationu
Ładunek białka
w pH = pI

Separacja białek za pomocą chromatografii jonowymiennej polega na
wykorzystaniu różnic w ładunku powierzchniowym cząsteczek białka
Wybór warunków chromatografii jonowymiennej:
• Białka zasadowe - pI białek przypada w pH zasadowym: stosujemy
kationit (polianion). Nanosi się białko w pH niższym niż pI białka, np.
białko pI 8,0 będzie kationem w pH 6,5 i zwiąże się do kationitu;
Elucja buforem o wyższym pH niż pH początkowe.
• Białka kwaśne – o pI w pH kwaśnym: stosujemy anionit (polikation).
Nanosimy białko w buforze o pH wyższym niż pI białka.
Np. białko o pI 4,5 będzie anionem w pH 5,7 i zwiąże się do anionitu.
Elucja: buforem o niższym pH niż pH początkowe.

SłabyMocny
Słabe wymieniacze anionowe zwykle tracą swój ładunek wraz ze wzrostem pH.
Przykład słabej grupy wymieniacza anionowego -DEAE (dietyloaminoetylowa).
Mocny Słaby
Słaby wymieniacz kationowy zawiera słaby kwas, który traci swój ładunek wraz ze spadkiem pH
Przykład słabej grupy wymieniacza kationowego –CM (karboksymetylowa).

Procedura
1. Równoważenie złoża
w kolumnie
2. Aplikacja próbki na
kolumnę
3. Elucja
❖ adsorpcja białek o
odpowiednim
ładunku
❖ desorpcja białek
związanych ze
złożem
4. Regeneracja złoża
Równoważenie kolumny
Adsorpcja próbki
Desorpcja próbki
Wymiana anionowa Wymiana kationowa

Elucja gradientem pH
– skokowym lub ciągłym
Elucja gradientem siły jonowej
Miksery pozwalają przygotować solwent
o odpowiednim składzie: np. pH, siły jonowej.
Pobierają solwenty z różnych naczyń i mieszająw nową kompozycję.
Liniowy gradient soli
Skokowy gradient soli
Sił
a j
on
ow
aS
iła
jo
no
wa
Objętość (ml)
Objętość (ml)

Zwana też chromatografią swoistej sorpcji
Wykorzystuje wzajemne powinowactwo biologiczne dwóch substancji.
Oddziaływanie w parze może mieć różny charakter, może to być np.:
- Hormon i receptor,
- Enzym i substrat,
- Enzym i inhibitor,
- Przeciwciało i antygen/hapten,
- Komplementarne odcinki kwasów nukleinowych,
- Kwas nukleinowy i białko,
- Lektyna i glikoproteina,
- Dopełniacz i przeciwciała z grupy IgG, itp.
W przypadku każdej pary oddziałujących cząsteczek, nie ma znaczenia,
która z nich zostanie wybrana jako ligand.

ligand
złoże
izolowana cząstkainne białka i zanieczyszczenia
przepływają swobodnie przez
kolumnę niezależnie od ich ładunku
czy masy.
Izolowane cząsteczki wymywane przez
dodatek wolnego ligandu,
konkurencyjnejncząsteczki, bądź przez
zmianę stężenia soli lub pH

Faza stacjonarna: warstwa cieczy opłaszczająca cząstki stałego złoża
Faza ruchoma: przepływająca przez kolumnę ciecz nie mieszająca się z fazą(cieczą) stacjonarną
Zasada rozdziału: różna rozpuszczalnośćskładników mieszaniny w obu nie mieszających się cieczach
Prawo podziału Nernsta

O rozdzielaniu decyduje różnica współczynników
podziału składników mieszaniny pomiędzy dwie
fazy ciekłe, tj. pomiędzy ciekłą fazą ruchomą i
ciekłą fazą stacjonarną osadzoną na nośniku.

Stała podziału Kd
Prawo podziału Nernsta, krótko prawo podziału określa sposób, w
jaki substancja rozpuszczona ulega podziałowi pomiędzy dwa nie
mieszające się rozpuszczalniki/ciecze tak, że w stanie równowagi
stosunek stężeń substancji rozpuszczonej w tych dwóch
rozpuszczalnikach jest stały w danej temperaturze i nie zależy od
ogólnego stężenia substancji
Jeżeli układ składa się z cieczy organicznej (org) i wody (w), wówczas prawo
podziału Nernsta wyraża się jako iloraz dwóch stężeń substancji rozpuszczonej:
gdzie:
- KX (org/w) - stała podziału substancji X pomiędzy fazy "1(org)" i "2(woda)"
(zw. też współczynnikiem podziału, zazwyczaj w skali logarytmicznej logP)
np. oktanol : woda.
- X org - stężenie substancji X w fazie "1(org)",
- X w - stężenie substancji rozpuszczonej w fazie "2(woda)".

Prawo podziału Nernsta może wyjaśnić zachowanie się danej substancji podczas
przenikania przez lipofilowe błony komórkowe oddzielające środowiska
wodne.
Lipofilowość jest ważną właściwością fizykochemiczą związków biologicznie
czynnych, wpływa na ich aktywność biologiczną, charakteryzuje substancje
czynne biologicznie, jak leki czy środki ochrony roślin
• umożliwia przewidywanie profilu wchłaniania, dystrybucji, metabolizmu i
wydalania (tzw. profil ADME), czyli zachowania się substancji w organizmie
człowieka po jej podaniu,
• pozwala określić możliwości wiązania z odpowiednim receptorem,
• podział substancji między fazę wodą i organiczną może stanowić model
podziału in vivo
Optymalne wchłanianie substancji z przewodu pokarmowego na drodze dyfuzji pasywnej po doustnym
podaniu :
1. Bardziej polarna substancja, słabsza przenikalność przez dwuwarstwę lipidową2. Bardziej niepolarna substancja jest słabiej rozpuszczalna w wodzie
3. Dobra jest równowaga między przenikalnością i rozpuszczalnością

Służy do rozdziału makrocząsteczek (białka, kwasy
nukleinowe) różniących się masą, szacowania ich masy,
do oddzielania makrocząsteczek od składników
niskocząsteczkowych np. sole (odsalanie) lub związki
używane do znakowania białek np. J125, fluoresceina;
do łagodnej zmiany warunków otoczenia białka (skład
elektrolitowy, pH).
Wykorzystuje mechanizm sorpcji zwany wykluczeniem;

Typ chromatografii podziałowej
Wypełnienie kolumny: porowaty żel
w postaci drobin poprzecinanych
kanałami o średnicy zmniejszającej sięw głębi ziarna
Faza stacjonarna – ciecz wewnątrz
ziaren żelu (wypełnienie kolumny),
Faza ruchoma – ciecz opływająca
ziarna żelu
Rozdzielanie zależne od wielkości
i kształtu cząsteczek w warunkach
eliminacji, sorpcji. Decyduje tylko
różnica czasu dyfuzji cząstek w
przestrzeni porów wypełnienia
kolumny.

Rozdział w kolumnach wypełnionych porowatym sieciowanym
wewnętrznie polimerem, np. poliakrylamid (Biogel), dekstran
(Sephadex), agaroza (Sepharose), w postaci ziaren o średnicy około
0,1 mm i o zdefiniowanej wielkości, czyli tzw. sita molekularne
W żelu małe cząsteczki wnikają do wnętrza ziaren, duże nie.
Droga (objętość, czas wypływu) dla każdego składnika jest nierówna.
Cząsteczki małe pokonuję najdłuższą drogę i dlatego wypływająnajpóźniej z kolumny.
Cząsteczki duże o efektywnej średnicy większej niż pory ziaren mająkrótszą drogę w żelu i wędrują najszybciej. Pojawiają się jako pierwsze
u wylotu kolumny.
Cząsteczki nie wiążą się z wypełniaczem kolumny i skład buforu nie
ma wpływu na rozdział

Wyniki rozdzielania zapisywane są w postaci wykresu,
składającego się z pików chromatograficznych, których
kształt odpowiada rozkładowi stężenia substancji
opuszczających kolejno kolumnę chromatograficzną.
Chromatogram dostarcza informacji:
jakościowych - na podstawie miejsca piku - o rodzaju
rozdzielanych substancji, strukturze molekularnej, ich
właściwościach fizykochemicznych - na podstawie liczby
pików, o liczbie składników w mieszaninie
ilościowych - wartość sygnału detektora, zmierzona jako
wysokość, albo powierzchnia piku, jest funkcją stężenia
bądź masy analitu w próbce dozowanej

rozdziałsłaby!
poprawa warunków
rozdziału
zastosowanie
elucji gradientowej
Rozdzielczość – zdolność do oddzielania
od siebie cząsteczek;

Przepływ solwentu przez kolumnę możliwy jest tylko wtedy, gdy pomiędzy wejściem i wyjściem kolumny panuje różnica ciśnień.
Tę różnicę ciśnień, w postaci ciśnienia hydrostatycznego, wywołuje zwykle pole grawitacyjne, lub
stosuje się specjalne pompy chromatograficzne, wymuszające znacznie większe przepływy, dzięki wyższym ciśnieniom do jakich mechanicznie sprężany jest solwent.

www.waters.com/webassets
schemat systemu HPLC
a – mikser gradientu d - kolumna
b – system pomp e - detektor
c – wstrzykiwanie próby f – wydruk danych
HPLC różni się od zwykłej chromatografii cieczowej ciśnieniem pod jakim
podawany jest eluent na kolumny.

Technika rozdzielania składników mieszanin na podstawie różnic w szybkości
ich migracji przez kolumnę zawierającą mikroziarnistą fazę stacjonarną.
Substancje są przenoszone przez kolumnę w strumieniu ciekłej fazy
ruchomej, poruszającej się pod wpływem ciśnienia, i są wykrywane w eluacie.
Metoda kolumnowa.
W HPLC stosowane są wszystkie mechanizmy sorpcji:
podział, adsorpcja, wymiana jonowa, wykluczenie, powinowactwa i chiralna.
Składniki rozdzielają się na podstawie szybkości migracji zależnej od
powinowactwa do faz.
Nośnik – ściana kolumny, drobnoziarniste ciało stałe.
Dozowanie próbki – ciekłe próbki i roztwory wprowadzane przez dozownik
(zawór) do fazy ruchomej na szczycie kolumny.
Identyfikacja – substancje rozdzielane wykrywane są w fazie ruchomej w
kolejności wypływu przez detektor – zależność stężenia od czasu.


Układ faz normalny: polarna faza stacjonarna (żel
krzemionkowy), eluent początkowo niepolarny ( pentan,
heksan, chloroform
Układ fazy odwróconej: niepolarna faza stacjonarna ( żel
krzemionkowy modyfikowany hydrofobowymi grupami
alkilowymi, np. oktylowymi), polarny eluent (acetinitryl, woda,
kwas octowy)
www.waters.com/webassets

Wysokość piku:
oznaczenie ilościowe
Identyfikacja
substancji: położenie
piku
www.waters.com/webassets

www.waters.com/webassets




Jednym z celów analitycznych chromatografii cienkowarstwowej jest rozdziałpróbki (mieszaniny) na pojedyncze składniki. W analizie nieznanej mieszaniny
na podstawie wartości Rf wzorców substancji i wartości Rf substancji
otrzymanych z rozdzielenia mieszaniny można określić jej skład jakościowy

Wraz z przesuwaniem się rozpuszczalnika przemieszczają się nałożone
składniki mieszaniny. Szybkość ich przemieszczania jest ich cechąindywidualną i zależy od powinowactwa składników do fazy stałej, podłoża
płytki (adsorbcja) i szybkości wymywania (desorpcja).
Dla substancji bezbarwnych stosuje się metodę wizualizacji ich miejsca
położenia na płytce chromatograficznej (wywoływanie chromatogramu)
W wyniku różnej szybkości migracji poszczególnych substancji w danych
warunkach, na płytce chromatograficznej powstaje seria plamek w różnej
odległości od linii startowej. Położenie plamek zaznacza się przez lekkie
obrysowanie ich krawędzi ołówkiem bezpośrednio po wywołaniu.
Następnie oblicza się współczynnik Rf (współczynnik retencji). Mierzy sięodległość środka plamki od linii startowej (w mm) i dzieli przez dystans -
pomiędzy linią startową i końcową też w mm. Pomiaru i obliczenia Rf
dokonuje się dla każdej plamki.

Co można powiedzieć o polarności związków 1 - 5, jeśli fazą stacjonarnąjest żel krzemionkowy a fazą ruchomą mieszanina cykloheksanu i
dichlorometanu (10 : 0,5; v:v)?

Chromatografia jest techniką rozdziału mieszanin substancji opartą na różnicach w szybkości poruszania się związków w dwóch fazach: stacjonarnej i ruchomej
Techniki chromatograficzne oparte są na procesach adsorpcji powierzchniowej lub podziału między dwie fazy ciekłe
W preparatyce białek istotne znaczenie mająchromatografia jonowymienna, powinowactwa i filtracja żelowa
Do celów analitycznych stosuje się wysokosprawnąchromatografię cieczową (HPLC) lub chromatografięcieczowo-gazową (GC)
Klasyczną techniką analityczną jest chromatografia cienkowarstwowa


Łańcuchy boczne aminokwasów kwaśnych i zasadowych odpowiadają za całkowity ładunek cząsteczki

Sumaryczny ładunek białka zależy od jego punktu izoelektrycznego i kwasowości środowiska

W polu elektrycznym ujemnie naładowane cząsteczki
( ) poruszają się w kierunku elektrody o ładunku
dodatnim ( ), a cząsteczki naładowane dodatnio
( ) w kierunku elektrody o ładunku ujemnym
( )
start
silnie ujemny
słabo ujemny
słabo dodatni
silnie dodatni
+-
Ładunek:

Elektroforeza – rozdział cząsteczek obdarzonych ładunkiem w polu elektrycznym

U osób zdrowych obraz elektroforetyczny frakcji białkowych jest stały
Analiza densytometryczna

Obraz elektroforetyczny (elektroforogram)
zmienia się w stanach patologicznych

1-chroniczny
2-ostry
gammapatie
stan zapalnymarskośćwątroby

Rutynowo nie rozdziela
się białek osocza.
Osocze zawiera
Fibrynogen między
frakcjami β i γ, w postaci
ostrego piku frakcji φ.
Może powodowaćto
trudności w identyfikacji
pików białka C-
reaktywnego (CRP) i/lub
części immunoglobulin
monoklonanych

Widoczny układ pasm białek zależy od sposobu barwienia i celu
badania
Zależnie od ruchliwości
elektroforetycznej powstaje
5 pasm izoenzymów
Izoenzymy dehydrogenazy mleczanowej

Lipoproteiny, transportowe kompleksy lipidów z białkami, różnią się składem, wielkością i gęstością

LDL=; VLDL=pre-; HDL=

Swoiste enzymy mogą ciąć DNA w ściśle zdefiniowanych miejscach (restricted sites)
Obraz elektroforetyczny pattern takich fragmentów jest unikalny dla każdego człowieka, jak odcisk palca
W obrazie fragmentów restrykcyjnych DNA wyraźnie widoczne jest pokrewieństwo, czasem też mutacje genomu

Dochodzenie
ojcostwa

Identyfikacja ofiar katastrof
i sprawców zbrodni

Denaturacja białka pod wpływem -merkaptoetanolui SDS (siarczanu dodecylu sodu)
Elektroforeza w żelu poliakryloamidowym w obecności SDS

Elektroforeza w żelu poliakryloamidowym daje lepszy rozdział frakcji (ma znacznie większązdolność rozdzielczą niż elektroforeza w agarozie

Kontrola czystości preparatów białkowych
Wyznaczanie masy cząsteczkowej białka
Identyfikacja niektórych mutacji/chorób

Ogniskowanie izoelektryczne – pierwszy wymiar
→pI 7,5
→pI 6,8
→pI 8,5
→pI 10,1
→pI 5,6
Stabilny gradient pH
W niskim pH białka mają ładunek dodatniW wysokim pH białka mają ładunek ujemny
W polu elektrycznym katoda i anoda przyciągają białka do miejsc pH = pI, gdzie stają się one obojętne
Białka przestały migrować, ponieważ znalazły się w miejscu, gdzie pH = pI

Drugi wymiar – SDS-PAGE

Proteomika funkcjonalna: poszukiwanie różnic w ekspresji białek pomiędzy stanami zdrowia i choroby
Proteomika – nauka zajmująca się badaniem białek – ich struktury,
sprawowanych przez nie funkcji i zależności między nimi, czyli proteomu

Cząsteczki obdarzone ładunkiem poruszająsię w zewnętrznym polu elektrycznym z szybkością zależną od ich ładunku, wielkości i kształtu
Obraz elektroforetyczny białek może ulegaćzmianie w wyniku procesów chorobowych
Obraz elektroforetyczny białek i lipoproteinmoże być wykorzystywany w diagnostyce
DNA-fingerprinting wykorzystuje się do identyfikacji osób oraz niektórych chorób