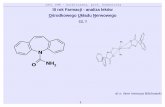
Leki OUN – neuroleptyki, LPD, anksjolityki III rok...
Transcript of Leki OUN – neuroleptyki, LPD, anksjolityki III rok...

Leki OUN – neuroleptyki, LPD, anksjolityki
III rok Farmacji - analiza lekówOśrodkowego Układu Nerwowego
cz. IIMateriały do ćwiczeń z Chemii Leków
dla studentów 3-go roku farmacji
dr n. farm Ireneusz Bilichowskiwersja 2013, poprawiona i uzupełniona
1

Leki OUN – neuroleptyki, LPD, anksjolityki
LEKI DZIAŁAJĄCE NA SFERĘ PSYCHICZNĄ LEKI PSYCHOTROPOWE
LEKI PSYCHOTROPOWE – są to substancje które wpływają na procesy psychiczne człowieka:– uspokajają, wpływają na nastrój, myślenie i zachowanieSą stosowane w schorzeniach psychiatrycznych, a także w celu modyfikowania emocji i zachowań w życiu codziennym.
Podział farmakologiczny
Neuroleptyki
Stosowane w terapii schizofrenii oraz w fazie maniakalnej psychoz z objawami pobudzenia i agresji.- Typowe neuroleptyki -Działają antagonistyczne do receptora D2-dopaminowegopochodne fenotiazyny, tioksantenu, butyrofenonu, difenylobutylopiperydyny- Neuroleptyki atypowe – agoniści receptora 5HT1A i hamują uwalnianie serotoninynależy do nich Buspiron
Przeciwdepresyjne - LPD
Podnoszące nastrój i napęd psychoruchowy, stosowane w leczeniu depresji. a) trójcykliczne LPD – hamujące wychwyt zwrotny noradrenaliny (NA) i/lub serotoniny (5-HT)b) inhibitory MAOc) sole litu
Przeciwlękowo-uspokajające (anksjolityki)
Leki tej grupy działają swoiście obniżając poziom lęku.a) pochodne 1,4-benzodiazepinyb) inne
Psychoanaleptyki
Przez wpływ na metabolizm komórek nerwowych mogą pośrednio aktywizować czynności psychiczne.Amfetamina i pochodne
2

Leki OUN – neuroleptyki, LPD, anksjolitykiLEKI PSYCHOTROPOWE
Pochodne fenotiazyny (trójcykliczne neuroleptyki)Działanie antypsychotyczne neuroleptyków uwarunkowane jest blokadą receptorów D2-dopaminowych w szlaku mezolimbicznym w oun. Posiadają także własności przeciwwymiotne i przeciwhistaminowe.
Większość neuroleptyków blokuje nie tylko receptory D2-dopaminowe, ale także receptory innych neuroprzekaźników. Wynika stąd szereg działań niepożądanych: blokada receptorów 1-adrenergicznych – spadek ciśnienia krwi, blokowanie receptorów histaminowych H1 – działanie uspokajające, D2 w podwzgórzu – wzrost stężenia prolaktyny.
Z wykładów Warunkiem działania neuroleptycznego pochodnych fenotiazyny jest zachowanie odległości pomiędzy atomami azotu w układzie fenotiazyny i łańcuchu bocznym, która powinna wynosić 3 atomy węgla. Siła działania zależy od wielkości podstawnika. Im większy podstawnik w pozycji 2, tym mniejsza dawka leku potrzebna jest do uzyskania efektu terapeutycznego.
Siła działania: H < Cl < OCH3 < CF3
3

Leki OUN – neuroleptyki, LPD, anksjolityki
5. NEUROLEPTYKI - POCHODNE FENOTIAZYNY I TIOKSANTENU5.1 Podstawowe struktury
Tabela 5.1 UKŁAD FENOTIAZYNY UKŁAD TIOKSANTENU
RODZAJ PODSTAWNIKA
• Alkiloamino podstawione • Piperydyloalkilo podstawione
PROMAZYNY MEPRAZYNY
PEKAZYNY RYDAZYNY
• Piperazynyalkilo podstawione
PERAZYNY
4
NC H 3
C H 3
NC H 3
C H 3C H 3N
C H 3
N
C H 3
N
NC H 3

Leki OUN – neuroleptyki, LPD, anksjolityki
5.2 Pochodne fenotiazyny - przykładowe związki farmakopealne
Tabela 5.2 Związki lecznicze pochodne fenotiazynyPochodne fenotiazyny EP 7.0
Promazyna Promazini Hydrochloridumchlorowoddorek 3- (10H-fenotiazyn-10-ylo)-N,N-dimetylopropano-1-aminyFP V, FP VI, EP 7.0PROMAZIN
Chlorpromazyna Chlorpromazini Hydrochloridumchlorowodorek 3-(2-Chloro-10H-fenotiazyn-10-ylo)-N,N-dimetylopropano-1-aminyFP V, FP VI, EP 7.0FENACTIL (Polfa, Warszawa)Obecnie w Polsce tylko: - krople , roztwór 40 mg/g - inj. 5 mg/ml
Prochlorperazyny maleinianProchlorperazini Maleas FP V, EP 6.0CHLORPERAZINUM
Trifluoperazyna Trifluoperazini HydrochloridumFP V, EP 6.0STELAZINE (GlaxoSmithKline)
5

Leki OUN – neuroleptyki, LPD, anksjolityki
Pochodne fenotiazyny - przykładowe związki farmakopealne c.d.
Perfenazyna PerphenazinumEP 7.0TRILAFON tab, TRILAFON ENANTHATE inj. (MSD ) - wycofane w 2013 r.
Tiorydazyna,ThioridazinumThioridazini hydrochloridum
10-[2-(1-Metylo-2-piperydynylo)etylo]-2-(metylotio)-10H-fenotiazyna
FP V, FP VI, EP 7.0THIORIDAZIN (Jelfa) – obecnie wyrejestrowany
Flufenazyna
Fluphenazini dihydrochloridum, Fluphenazini decanoas EP 7.0MIRENIL (Jelfa S.A.) - wyjerestrowany
Lewomeproazyna
Levomepromazini hydrochloridumLevomepromazini Maleaschlorowodorek (2R)-3-(2-metoksy-10H-fenotiazyn-10-ylo)-N,N,2-trimetylopropano-1-aminy FP V, EP 7.0TISERCIN
6

Leki OUN – neuroleptyki, LPD, anksjolityki
5.3 Pochodne fenotiazyny – o działaniu przeciwwymiotnymAntagoniści receptorów D2
Pochodne fenotiazyny wykazują słabe działanie przeciwwymiotne. Działanie to można zwiększyć wprowadzając w pozycję 2 pierścienia fenotiazynowego podstawnik etylenotiolowy lub metylosulfonowy – patrz wykłady.
Pochodne fenotiazyny o działaniu przeciwwymiotnym
Nie farmakopealnyTioperazyna, Thioproperazine (MAJEPTYL, Sanofi-Aventis )
TietylperazynaThiethylperazine maleate (TORECAN, Krka SLO)
USP 29
Nie farmakopealnyMetopimazyna, Metopimazine, (VOGALEN, Schwarz Pharma; Sanofi-Aventis )
7

Leki OUN – neuroleptyki, LPD, anksjolityki
5.4 NEUROLEPTYKI - Pochodne tioksantenu
Chlorprotyksen, Chlorprotixeni Hydrochloridum,(Z)-3-(2-Chloro-9H-tioksanten-9-ylidieno)-N,N-dimetylopropano-1-aminy chlorowodorekFP V, EP 7.0TARACTAN (Roche Lab.)
Flupentyksol, Flupentixoli dihydrochloridum, FP V, EP 67.0FLUANXOLFLUANXOL Depot (Lundbeck DK)
2-[4-[3[(EZ)-2-(Trifluorometylo)-9H-tioksanten-9-ylidieno]propylo]piperazyn-1-ylo]etanolu dichlorowodorek
Obecność wiązania podwójnego w układzie tioksantenu warunkuje izomerię geometryczną. Izomer cis działa silniej niż trans. W farmakopei nazwa chemiczna określa który izomer jest substancją czynną (API).
Uważa się że pochodne tioksantenu są bardziej bezpieczne od poch. fenotiazyny. Działają antagonistycznie na receptory D1 i D2 dopaminowe.Estry z kwasem dekanowym są bardziej lipofilowe i umożliwiają uwalnianie substancji czynnej z tkanki tłuszczowej w miejscu iniekcji (ang. - depot).
Klopentyksol, jako ester z kwasem dekanowymZUKLOPENTYKSOLU DEKANONIAN, EP 7.0Zuclopenthixoli decanoas, 2-[4-[3[(9Z)-2-chloro-9H-tioksanten-9-ylidieno]propylo]piperazyn-1-ylo]etanolu dekanonianCLOPIXOL tab. (Lundbeck DK)
8

Leki OUN – neuroleptyki, LPD, anksjolityki
5.5 NEUROLEPTYKI - pochodne butyrofenonuPochodne butyrofenonu z EP 7.0
HALOPERYDOLHaloperidolum 4-[4-(4-chlorofenylo)-4-hydroksypiperydyn-1-ylo]-1-(4-fluorofenylo)butan-1-onFP V, FP VI, EP 7.0
Bromperydol BromperidolumEP 7.0
Bromperydolu dekanonian, Bromperidoli decanoas, EP 7.0Pochodne z atomem bromu działają silniej, w Polsce nie zarejestrowany.
HALOPERYDOLU DEKANONIAN Haloperidoli decanoas, EP 7.0Ester dekanowy haloperydolu
Droperydol DroperidolumEP 7.0 m.cz. 379,4
Droperidol – jest stosowany w neuroleptoanalgezji razem z pochodnymi Fentanylu.
Pochodne butyrofenonu działają silniej od pochodnych fenotiazyny.Mają silne działanie niepożądane na układ pozapiramidowy, mogą nasilać stany depresyjne, działają sedatywnie.
Kwas -aminomasłowy
9

Leki OUN – neuroleptyki, LPD, anksjolityki
Pochodne butyrofenonu z EP 7.0
Benperydol, BenperidolumEP 7.0m.cz. 381,4
W Polsce nie zarejestrowany.
10

Leki OUN – neuroleptyki, LPD, anksjolityki
5.6 NEUROLEPTYKI - pochodne dibenzoepiny i difenylobutylopiperydyny
KlozapinaClozapinum8-Chloro-11-(4-metylopiperazyn-1-ylo)-5H-dibenzo[b,e]-[1,4]diazepinaEP 7.0LEPONEX (Novartis Pharma)KLOZAPOL (Egis Pharm. PLC)
Wykazuje mniejszą aktywność antagonistyczną do receptorów dopaminowych D2, co powoduje mniejsze efekty pozapiramidowe. Pomocniczo stosowana w padaczce opornej na inne leki.
FluspirylenFluspirylenum
EP 7.0IMAP (Janssen Pharm.)
8-[4,4-bis(4-fluorofenylo)butylo]-1-fenylo-1,3,8-triazaspiro-[4,5]dekan-4-on
5.7 NEUROLEPTYKI atypoweBuspironBuspironi HydrochloridumEP 7.0SPAMILAN (Egis Pharm. PLC)
Częściowy agonista receptora 5HT1A, jest antagonistą receptorów D2 . Nie wykazuje właściwości przeciwdrgawkowych i uspokajających.
Pochodne benzamidu
SulpirydSulpirydumEP 7.0SULPIRYD (Pliva -Kraków)
11

Leki OUN – neuroleptyki, LPD, anksjolityki
6.0 Leki przeciwdepresyjne LPD 6.1 – trójpierścieniowe pochodne dibenzoazepiny
TLPD – trójpierścieniowe leki przeciwdepresyjne
IMIPRAMINA Imipramini hydrochloridum5-[3-(Dimetyloamino)-propylo]-10,11-dihydro-5H-dibenzo[b,f]azepinaFP V, FP VI, EP 7.0TOFRANIL (Novartis)
I - generacjaPierwszy trójcykliczny antydepresant wprowadzony w latach 1950 r przez Ciba-Geigy. Obecnie już nie stosowany
Opipramol,Opipramoli hydrochloridum PRAMOLAN (Polpharma )FP V, FP VI5-[3-(N´-β-Hydroksyetylopiperazyno)-propylo]-5H-dibenzo[b,f]azepina
AMITRYPTYLINAAmitryptylini hydrochloridum3-(10,11-dihydro-5H-dibenzo[a,d]cycloheptano-5-ylideno)-N,N-dimetylpropano-1-aminy chlorowodorek
FP V, FP VI, EP 7.0
Nie selektywny inhibitor wychwytu zwrotnego monoaminy.
DOKSEPINA Doxepini hydrochloridum (E)-3-(Dibenzo[b,e]oksepin-11(6H)-ylidieno)-N,N-dimetylopropano-1-aminy chlorowodorekFP V, FP VI, EP 7.0SINEQUAN (Pfizer)
12

Leki OUN – neuroleptyki, LPD, anksjolityki
6.2 Leki przeciwdepresyjne, inne
KlomipraminaClomipramini hydrochloridum3-(3-Chloro-10,11-dihydro-5H-dibenzo[b,f]azepino-5-yl)-N,N-dimetylopropano-1-aminy chlorowodorekEP 7.0ANAFRANIL (Novartis)
FluoksetynaFluoxetini hydrochloridumjako racematEP 7.0PROZAC (Eli Lilly)
3(RS)-N-Metylo-3-fenylo-3-[4-(trifluorometylo)fenoksy]propan-1-aminy chlorowodorekSelektywny inhibitor wychwytu zwrotnego serotoniny.
MianserynaMianserini hydrochloridumchlorowodorek (RS)-2-metylo-1,2,3,3,10,14b-heksahydrodibenzo[c,f]pirazyno[1,2-a]azepinyEP 7.0LERIVON, MIANSEC (Jelfa S.A.)
13

Leki OUN – neuroleptyki, LPD, anksjolityki
Leki przeciwdepresyjne6.3 Inhibitory MAO 6.4 Sole litu stosowane w profilaktyce psychoz
afektywnych
ISOCARBOXAZID, EP 6.0Izokarboksazyd (MARPLAN, Hoffman-LaRoche)
Pierwsza generacja. Nieselektywny i nieodwracalny inhibitor MAO. Nie stosowany !
Farmakopealne sole litu:
1) LITHII CARBONAS,
Litu węglan, Li2CO3 ,
2) LITHII CITRAS,
Litu cytrynian, LI3+ [HO-C-(COO)(CH2COO)2]3- ,
MOCLOBEMID, Moklobemid (MANERIX, Hoffman-LaRocheMOBEMID, Jelfa S.A.)Trzecia generacja. Selektywny i odwracalny inhibitor MAO.
14

Leki OUN – neuroleptyki, LPD, anksjolitykiAnaliza zasad heterocyklicznych i soli zasad organicznych
Pochodne Fenotiazyny Własności, analiza jakościowa
O charakterze zasadowym pochodnych fenotiazyny decyduje trzeciorzędowa grupa aminowa lub atom azotu w alifatycznym
pierścieniu heterocyklicznym.
Atom azotu w układzie fenotiazyny nie ma żadnego znaczenia dla charakteru zasadowego ponieważ pierścienie aromatyczne i
elektrofilowy atom siarki wykazują efekt elektronossący do elektronów atomu azotu
Stosowane są one w najczęściej w postaci soli jako chlorowodorki lub maleiniany, co poprawia ich rozpuszczalność.
15
S
N
NC H 3
C H 3
S
N
N
C l
N

Leki OUN – neuroleptyki, LPD, anksjolityki
Analiza zasad heterocyklicznych i soli zasad organicznych
Leki psychotropowe stanowią grupę związków zaliczanych do zasad organicznych lub zasad heterocyklicznych (atom azotu występuje w pierścieniu). W analizie jakościowej soli zasad organicznych znaczenie mają reakcje umożliwiające wykrycie zasady organicznej i anionu.
Większość zasad organicznych trudno rozpuszcza się w wodzie. Ale badanie rozpuszczalności w wodzie nie zawsze umożliwia
rozróżnienie wolnych zasad od ich soli. Użycie roztworu silnej zasady nieorganicznej ( 0,5 mol/l NaOH) pozwala na wydzielenie wolnej zasady.Roztwory wodne wolnych zasad mają często pH powyżej 7.
Odczyn roztworów soli waha się od pH 7 do 3, w zależności od mocy zasady i kwasu.
W badaniach wst ępnych sto suje si ę reakcje og ólne z:odczynnikiem Dragendorffa – osady barwy czerwono-pomarańczowej
roztwór jodu w jodku potasu – tworzy nierozpuszczalne w wodzie nadjodki
nasycony roztwór kwasu pikrynowego – pikryniany barwy żółtej – tworzenie pikrynianów jest harakterystyczne dla zasad
heterocyklicznych. Aminy aromatyczne nie tworzą trwałych soli z kwasami.kwas krzemowolframowy H8[Si(W2O7)6] x H2O – białe osady
kwas fosforomolibdenowy H3[P(Mo3O10)4] – białe osady
sól Reineckego NH4[Cr(SCN)4(NH3)2] x H2O – trudno rozpuszczalne związki o
barwie czerwonofioletowej
16

Leki OUN – neuroleptyki, LPD, anksjolityki
Pochodne Fenotiazyny - stężony 96% H2SO4
stężony 96% H2SO4 który dzięki własnościom utleniającym daje barwne produkty z licznymi związkami. Jest on także składnikiem wielu odczynników:
odcz. Erdmana - 20 ml 96% H2SO4 + 0,5 ml 0,15% HNO3
odcz. Fredego - 96% H2SO4 z 0,5% molibdenianu amonu
odcz. Mandelina - 96% H2SO4 z 0,5% wanadynianu amonu
odcz. Marquisa – 3 ml 96% H2SO4 z 3 kroplami aldehydu mrówkowego
17

Leki OUN – neuroleptyki, LPD, anksjolitykiNEUROLEPTYKI - barwne testy*
Chlorpromazyna Chlorprotyksen Amitryptylina ImipraminaFormaldehyd /H2SO4 czerwony –
w fiolet
czerwony
pomarańczowa fluorescencja w UV
Mandelin zielony –
w fiolet
czerwony brąz w zielony niebieski
Marquis fioletowo –
różowy
czerwony -
w pomarańcz
brązowo - pomarańcz niebieski
Stęż. H2SO4 czerwony pomarańczowa fluorescencja w UV
pomarańcz niebieski
Stęż. HNO3 czerwony niebieskiDragendorff + + + +
Odczynnik Dragendorffa KBiJ4 Jest to azotan bizmutu z jodkiem potasu, Bi(NO3)3 + KJ w 10mol /dm3 HClWykonanie badania:Rozpuścić badaną substancję w 3 kroplach 2 M HCl, dodać 2-3 ml odczynnika, ewentualnie rozcieńczć wodą do 5 – 10 ml.Reakcja dodatnia – osad pomarańczowy, czerwono-pomarańczowy do brązowego dają aminy I, II, III i IV rzędowe.
[zasada-H+][BiJ4-]
*) Clarke's Analysis of Drugs and Poisons, Pharmaceutical Press 2004Consulting Editors: Anthony C Moffat, M David Osselton, Brian WiddopManaging Editor: Laurent Y Galichet
książka dostępna w wersji elektronicznej na stronach Biblioteki Głównej UMhttp://www.bg.am.lodz.pl/ baza danych: MedicinesComplete
18

Leki OUN – neuroleptyki, LPD, anksjolityki
Reakcje pierścienia fenotiazynowego pod wpływem środków utleniających: 96% H2SO4, 65% HNO3, 1% FeCl3, HIO4, Ce(SO4)2
19
S
N
R
R
S
N
R
R
S
N
R
R
S+
N
R
R
OH
S
N
R
R
O
W zależności od podstawników R1 i R2 wolne rodniki mogą przyjmować różne zabarwienie:
promazyna pomarańczowechlorpromazyna – czerwonetiorydazyna – niebieskie
skrypt strona 82

Leki OUN – neuroleptyki, LPD, anksjolityki
Pochodne fenotiazyny – zestawienie reakcji i własności(1) Większość związków z tej grupy jest chlorowodorkami są więc rozpuszczalne w wodzie i dają pozytywną reakcję na chlorowiec
związany jonowo
(2) Niektóre związki dają reakcję na chlorowiec związany kowalencyjnie
(3) Pod wpływem środków utleniających, np. 96% H2SO4, 65%HNO3, 1% FeCl3, utleniają się tworząc charakterystycznie zabarwione
pochodne.
Barwną reakcję dają pochodne fenotiazyny, tioksantenu, trójpierścieniowe leki przeciwdepresyjne (Imipramina, Amitryptylina,
Doksepina, Opipramol). Kolor i intensywność zależą od związku.
(4) Fenotiazyny po przeprowadzeniu w wolną zasadę dają sole z kwasem pikrynowym o charakterystycznych temperaturach topienia
(5) tworzą w środowisku kwaśnym sole heteropolikwasami np. z kwasem krzemowolframowym 10% r. H8[Si(W2O7)6] x H2O .
W FP IV ta reakcja służyła jako wagowa metoda oznaczania pochodnych Fenotiazyny
(6) Do rozróżnienia tych związków wykorzystuje się temperatury topnienia wolnych zasad i pikrynianów
(7) Wiarygodnym sposobem rozróżnienia tych związków jest wykonanie widma IR i H1NMR
np. odróżnienie promazyny i prometazyny (Diphergan)
(8) Jedną z metod badania pochodnych fenotiazyny w Europejskiej Farmakopei jest chromatografia cienkowarstwowa (rozdz. 2.2.27)
i chromatografia cieczowa (rozdz. 2.2.29). Wymagane są wzorce.
20

Leki OUN – neuroleptyki, LPD, anksjolityki
promazyna prometazyna
Temperatury topnienia zasad i pochodnych pikrynianów niektórych związków
Zasada pikrynian
Chlorpromazyny HCL 194 – 197 °C 172 – 174 °C
Imipramina HCL 169 – 173 °C 140 – 142 °C
Promazyna HCL 177 – 181 °C 144 – 147 °C
Prometazyna HCL 218 – 225 °C 158 - 161 °C
Haloperidol 147 – 152 °C 226 – 227 °C
21

Leki OUN – neuroleptyki, LPD, anksjolityki
Widma UV – chlorpromazyna, promazyna rozróżnienie
Cz – chlorpromazyny chlorowodorek w Hcl 3,6 g/l λmaksimum 254 i 304 nm
Z, N – promazyny chlorowodorek w Hcl 3,6 g/l λmaksimum 252 i 302 nm
Chlorpromazyna ma przesunięte maksimum absorpcji o 2 nm
z powodu obecności atomu chloru w pierścieniu.
22

Leki OUN – neuroleptyki, LPD, anksjolityki
Widma IR – promazyny
Chlorpromazyny chlorowodorek,tabletka w KBr
Prometazyny chlorowodorek, tabletka w KBr
23

Leki OUN – neuroleptyki, LPD, anksjolityki
Analiza ilościowa pochodnych fenotiazyny
W analizie ilościowej soli zasad organicznych ogólne zastosowanie znalazła metoda acydymetryczna w środowisku niewodnym oraz spektrofotometria w UV. Sole zawierające jony halogenkowe można oznaczać argentometrycznie metodą Volharda – obecnie metoda nie polecana.Niektóre związki z tej grupy można oznaczyć wykorzystując ich zdolność do tworzenia trudno rozpuszczalnych połączeń z kwasem krzemowolframowym lub solą Reineckego NH4[Cr(SCN)4(NH3)2] x H2O (metody wagowe wg FP IV, obecnie nie polecane).
1. acydymetrycznie w środowisku niewodnym - chlorowodorki, w kwasie octowym dodając octanu rtęci, i miareczkując kwasem nadchlorowym wobec zieleni malachitowej.
R-NH3+Cl- + (CH3COO)2Hg R-NH3
+ CH3COO- + HgCl2 (1)
R-NH3 + CH3COO- + CH3COOH2+ClO4
- R-NH3+ ClO4- + 2CH3COOH (2)
FPV poleca oznaczanie Chlorowodorku Chlorpromazyny miareczkując kwasem nadchlorowym po rozpuszczeniu w mieszaninie bezwodnika octowego i kwasu octowego, wobec zieleni malachitowej.
Gramorównoważnik = 1 gramocząsteczka
Metoda w środowisku niewodnym jest stosowana do oznaczania pochodnych fenotiazyny i tioksantenu, obecnie coraz częściej punkt końcowy
miareczkowania wyznacza się potencjometrycznie.
2. acydymetrycznie w środowisku niewodnym – sole z kwasem maleinowym:
miareczkujemy bezpośrednio kwasem nadchlorowym w kwasie octowym
[R-NH3+] [HOOC-CH=CH-COO- ] + CH3COOH2
+ClO4- R-NH3
+ ClO4- + HOOC-CH=CH-COOH
+ CH3COOH
EP 7.0 - lewomepromazyny maleinian- prochlorperazyny maleinian
24

Leki OUN – neuroleptyki, LPD, anksjolityki
3. Acydymetrycznie w środowisku niewodnym wg farmakopei europejskiej EP 7.0 Bezpośrednie miareczkowanie chlorowodorku aminy (np. fenotiazyny lub tioksantenu) silną zasadą (0,1 mol/l NaOH) w etanolu jako
rozpuszczalniku.
Chlorowodorki zasad często zawierają śladowe ilości wolnego HCl, i w rozpuszczalniku niewodnym obserwujemy dwa punkty przegięcia
krzywej miareczkowania (pKa HCl < pKa chlorowodorku zasady). Trudno jest oznaczyć ilościowo śladowe ilości HCl dlatego do roztworu
próbki dodaje się niewielką ilość kwasu solnego. Wtedy pierwszy punkt przegięcia jest bardziej widoczny.
PK miareczkowania wyznaczamy potencjometrycznie.
Ważne jest użycie w tym przypadku roztworu NaOH wolnego od węglanów.
Przepis:Odważyć próbkę związku z dokładnością do 0,1 mg i rozpuścić w 50 ml etanolu.Dodać pipetą 5 ml roztw. HCl 0,01mol/l, włożyć element mieszający i miareczkować roztworem 0,1 mol/l NaOH.W metodzie klasycznej dodawać równe objętości co 0,2 ml i notować wartość potencjału lub pH, lub używając tittratora.Odczytać objętość dodaną pomiędzy dwoma punktami przegięcia.
Równanie reakcji
R-NH3+Cl- + NaOH R-NH2
+ NaCl + H2O
Wg EP 7.0 tą metodą oznaczane są: chlorpromazyny HCl, chlorprotyksenu HCl,
promazyny HCl, prometazyny HCl, trifluoroperazyny HCl, lewomepromazyny HCl
4. spektrofotometrycznie w UV w 0,1 mol/l HCl
25
-0,5 0,5 1,5 2,5 3,5 4,5 5,5 6,5 7,5 8,5 9,5 10,50
50
100
150
200
250
300
350
400
450
500
Ephedrine HCl EP 6.0
SEM [mV]
V [ml] (NaOH 0,1 mol/l])

Leki OUN – neuroleptyki, LPD, anksjolityki
8. NEUROLEPTYKI - pochodne butyroferonu
Pochodne butyroferonu z EP 7.0
Haloperydol,Haloperidolum4-[4(4(chlorofenylo)-4-hydroksypiperydyno]-4'-fluorobutyroferon
EP 7.0
Haloperydolu dekanonian, Haloperidoli decanoas, EP 7.0
Droperydol, Droperidolum
EP 7.0
inj. 2,5mg/ml
1-{1-[4-(4-fluorofenylo)-4-oxobutylo]-1,2,5,6-tetrahydropiridin-4-ylo]-1,3-dihydro-2H-benzimidazol-2-on
Neuroleptoanalgezja – podanie leku neuroleptycznego równocześnie z opioidem – co prowadzi do stanu w którym pacjent jest uspokojony i pozbawiony lęku, i obojetny w stosunku do otoczenia. Nie zawsze dochodzi do zaśnięcia, nie następuje pełne zwiotczenie mięśni i tłumienie odruchów.
Haloperidol Silny neuroleptyk - 50 razy silniejsze działanie od chloropromazyny, Benperydol - 75 razy !Wykazuje silne działanie uspokajające i przeciwpsychotyczne. W schizofrenii działa silnie na objawy wytwórcze. U osób pobudzonych zmniejsza napęd psychoruchowy i niepokój.Wykazuje także działanie przeciwwymiotne oraz hamuje skutecznie nudności i czkawkę.Jest to jeden z najsilniejszych z tej grupy, silniej od haloperidolu działają związki podstawione bromem zamiast chlorem.
26

Leki OUN – neuroleptyki, LPD, anksjolityki
Pochodne butyrofenonu – reakcje
Haloperidol FPV, EP 7.04-[4(4(chlorofenylo)-4-hydroksypiperydyno]-4'-fluorobutyroferonWłasności: Trudno rozpuszcza się w metanolu, nie rozpuszcza się w wodzieReakcje tożsamościowe:1) Z kwasem pikrynowym - Pikrynian t.t 226 – 227 °C2) Reakcja z 1,3 dinitrobenzenem (Reakcja Zimmermana) – reakcja tożsamościowa w EP 6.0 dla pochodnych butyroferonu powstaje zabarwienie czerwone lub fioletowe po dodaniu metanolowego roztworu KOH
Zawartość: Acydymetrycznie w środowisku niewodnym jak wolną zasadę, miareczkując 0,1 mol/l kwasem nadchlorowym wobec fioletu krystalicznego lub potencjometrycznie.
27

Leki OUN – neuroleptyki, LPD, anksjolityki
Leki przeciwdepresyjne - LPD - pochodne dibenzoazepiny i dibenzocykloheptadienuIMIPRAMINY CHLOROWODOREKImipramini Hydrochloridum 5-[3-(Dimetyloamino)-propylo]-10,11-dihydro-5H-dibenzo[b,f]azepinaFP V, FP VI, EP 7.0
Rozpuszcza się w wodzie i metanolu.
Tożsamość:
1) 65% HNO3 – niebieskie zabarwienie
2) 96% H2SO4 – niebieskie zabarwienie
3) Odcz. Mandelina – niebieskie
4) pikrynian t.t. 140-142 °C
5) Roztwór wodny – reakcja na chlorki
Zawartość: acydymetrycznie w środowisku niewodnym, wobec fioletu krystalicznego lub potencjometrycznie
AMITRYPTYLINY CHLOROWODOREKAmitryptylini Hydrochloridum3-(10,11-dihydro-5H-dibenzo[a,d]cycloheptano-5-ylideno)-N,N-dimetylpropan-1-aminy chlorowodorekFP V, FP VI, EP 7.0
Rozpuszcza się w wodzie i metanolu.
Tożsamość:
1) 96% H2SO4 – czerwono pomarańczowe zabarwienie
2) Odcz. Marquisa – brązowo-pomarańcz.
3) Odcz. Mandelina – brąz – w zielony
4) Roztwór wodny – reakcja na chlorki
Zawartość: acydymetrycznie w środowisku niewodnym, wobec fioletu krystalicznego lub potencjometrycznie
28

Leki OUN – neuroleptyki, LPD, anksjolityki
7. Leki Anksjolityczne 7.1 Pochodne 1,4-benzodiazepiny
Pochodne benzodiazepiny 1,4 są słabymi zasadami jednoprotonowymi. Ich właściwości zasadowe wynikają głównie z obecności I
i II-rzędowego azotu w pozycji 1. Drugi atom azotu w pozycji 4 wykazuje słabsze własności zasadowe ( hybrydyzacja sp2).
29

Leki OUN – neuroleptyki, LPD, anksjolityki
7.1 Pochodne 1,4benzodiazepiny – związki farmakopealnePochodne 1,4 benzodiazepiny
R1 – CH3, H
R2 – OH, H
R3 – o, m., p. - F, Cl
R4 – NO2, Br, Cl, F, H
DIAZEPAM Diazepamum 7-Chloro-1,3-dihydro-5-fenylo-1-metylo-2H-1,4-benzodiazepin-2-onFP V, EP 7.0RELANIUM
1959 r. - synteza Leon Sternbach, 1963 r. - wprowadzony do lecznictwa pod nazwą Valium (Hoffman-La Roche)
Chlordiazepoksydu chlorowodorekChlordiazepoxidi hydrochloridum4-Tlenek-7-chloro-2-metyloamino-5-fenylo-3H-1,4-benzodiazepiny, chlorowodorek
FP V, FP VI, EP 7.0ELENIUM
1958 r. - synteza
NITRAZEPAMNitrazepamum5-fenylo-7-nitro-1,3-dihydro-1H-1,4-benzodiazepin-2-onFP V, EP 7.0
KLONAZEPAMClonazepamum5-(2-chlorofenylo)-7-nitro-1,3-dihydro-2H-1,4-benzodiazepin-2-onFP V, EP 7.0
30

Leki OUN – neuroleptyki, LPD, anksjolityki
Pochodne 1,4 benzodiazepiny
OKSAZEPAMOXAZEPAMUM(3RS)-7-Chloro-3-hydroksy-5-fenylo-1,3-dihydro-2H-1,4-benzodiazepin-2-on FP V, EP 7.0OXAZEPAM
ALPRAZOLAMAlprazolamum
EP 7.0XANAX
FLUNITRAZEPAMFlunitrazepamum
EP 7.0ROHYPNOL (Glaxo)
Obecnie w Polsce wyrejestrowany
Triazolam
USP 24
MEDAZEPAM
RUDOTEL (Merckle GmbH)
CHLORAZEPAMDikali clorazepas1H-1,4-Benzodiazepine-3-carboxylic acid, 7-chloro-2,3-dihydro-2-oxo-5-phenyl-, potassium salt with potassium hydroxide (1:1)TRANXENE(Sanofi-Aventis)
31

Leki OUN – neuroleptyki, LPD, anksjolityki
Pochodne 1,4benzodiazepiny – własności zasadowe
Zasadowość
Nitrazepam i klonazepam mają własności kwaśne ze wględu na obecność grupy nitrowej i elektronossący charakter grupy C=O przy C2.
32
NH
NO2N
O
NH
NO2N
O
Cl
Nitrazepam
N
N
O
Cl
CH3
NH
N
O
OH
N
N
NHCH 3
ClO
Diazepam Oksazepam Elenium
Klonazepam

Leki OUN – neuroleptyki, LPD, anksjolityki
7.2 Pochodne 1,4benzodiazepiny – widma IR
W widmach absorpcji w podczerwieni pochodnych 1,4benzodiazepiny obserwujemy
liczne pasma absorpcji charakterystyczne dla zasad herterocyklicznych – grupy NH, oraz dla charakterystycznych podstawników.
Klonazepam: [cm-1] νNH /3200-3100/, νCH /3076, 3056/, νC=O /1696/, νNO2 /asym. 1540, sym. 1339/
33

Leki OUN – neuroleptyki, LPD, anksjolityki
IR
Widmo IR Clonazepam, w KBr
Widmo IR – Diazepam w KBr
34
3103
.2
2969
.3
3211
.3
1692
.516
14.6
1337
.512
56.2
1487
.614
01.0
869.
2
750.
2
869.
2
1100
.010
15.3
844.
8
558.
5
5001000150020002500300035004000
-20
0
20
40
60
80
Operator: A.Sut Wed Apr 22 12:53:47:88 2009 IJB-CLON
Wavenumbers
3428
.2
2914
.8
3071
.7
2970
.4
1684
.516
02.6
1482
.3
1313
.9 1127
.2
706.
6813.
7
1399
.5 1200
.6
1073
.9
886.
2
582.
155
1.9
1559
.15001000150020002500300035004000
50
60
70
80
Operator: A.Sut Wed Apr 22 12:45:31:81 2009 IJB-DIAZ
Wavenumbers

Leki OUN – neuroleptyki, LPD, anksjolityki
7.3 Pochodne 1,4benzodiazepiny Reakcje ogólne Pochodne 1,4-benzodiazepiny dają pozytywną reakcję
(1) z kwasem pikrynowym w środowisku bezwodnym tworzą intensywnie żółto zabarwione sole
( λmaks = 445 nm daje jon pikrynowy).
(2) z solą Reineckego NH4[Cr(SCN)4(NH3)2] x H2O (czterorodanodwuamonochromianamonowy) tworzą w środowisku kwaśnym
trudno rozpuszczalne kompleksy - różowe sole, które są rozpuszczalne w acetonie co jest wykorzystane w metodzie
kolorymetrycznej oznaczania
[BH]+ + [Cr(SCN)4(NH3)2]- BH[Cr(SCN)4(NH3)2]
Sposób wykonania:Rozpuścić badany związek w niewielkiej ilości 10% HCl, dodać 1% metanolowego roztworu soli Reineckiego. Powstaje różowy osad. Osad przesączyć i rozpuścić w acetonie, powstaje różowe zabarwienie ( λ max ok. 520 nm)
(3) tworzą także w środowisku kwaśnym osady z kwasem krzemowolframowym
H8[Si(W2O7)6] x H2O
35

Leki OUN – neuroleptyki, LPD, anksjolityki
7.4 Pochodne 1,4benzodiazepiny – REAKCJE SZCZEGÓŁOWE
(4) próba Zimmermana - charakterystyczna dla aktywnej grupy CH2 przy C=O .
Wykonanie: do metanolowego roztworu badanej substancji dodać kryształ 1,3-dinitrobenzenu (lub 0,5 ml roztworu)i
następnie 1-2 krople 15% KOH. Powstaje pomarańczowe zabarwienie.
Reakcji nie daje oksazepam i chlordiazepoksyd (elenium). !
36

Leki OUN – neuroleptyki, LPD, anksjolityki
Pochodne 1,4benzodiazepiny – REAKCJE SZCZEGÓŁOWE
próba Zimmermana Sposób wykonania:Rozpuścić ok 10 mg substancji w 5 ml metanolu, dodać 0,5 ml r. 1,3-dinitrobenzenu, nastepnie 0,5 ml metanolowego r. KOH 2 mol/l, powstaje pomarańczowe zabarwienie.
37

Leki OUN – neuroleptyki, LPD, anksjolityki
Pochodne 1,4benzodiazepiny – REAKCJE SZCZEGÓŁOWE
(5) Nitrazepam i klonazepam ze względu na obecność grupy nitrowej mają zwiększony charakter kwaśny. W środowisku
zasadowym tworzą stabilizowane rezonansem aniony o zabarwieniu żółtym
Wykonanie: 10 mg substancji rozpuścić w 2 mL Metanolu (lekko ogrzać) i dodać 2 krople 10 % NaOH.
38

Leki OUN – neuroleptyki, LPD, anksjolityki
Pochodne 1,4benzodiazepiny – REAKCJE SZCZEGÓŁOWE
(6) 1,4-benzodiazepiny hydrolizują w środowisku kwaśnym dając odpowiednie pochodne benzofenonu. Obecność aminy I-rzędowej można wykryć za pomocą reakcji diazowania i sprzęgania z naftyloetylenodiaminą, obecność aminokwasu można wykryć w reakcji z ninhydryną.
Hydroliza diazepamu
Przebieg hydrolizy uzależniony jest od rodzaju związku i warunków prowadzenia reakcji.
39
N
NCl
OCH3
N
NH2
Cl
O
CH3
O
NH
OCl
CH3
H2O / H+
COOH
NH2

Leki OUN – neuroleptyki, LPD, anksjolityki
7.5 Analiza ilościowa pochodnych 1,4benzodiazepiny
Diazepam, nitrazepam, oksazepam oznaczamy acydymetrycznie w środowisku niewodnym, jak wolne zasady. Po rozpuszczeniu substancji w kwasie octowym, miareczkujemy kwasem nadchlorowym wobec zieleni malachitowej, lub potencjometrycznie.
40

Leki OUN – neuroleptyki, LPD, anksjolityki
Benzodiazepiny metody oznaczania Natomiast chlordiazepoksyd (Elenium) jak chlorowodorki oznaczamy w środowisku niewodnym dodając octanu rtęciowego.
Wg EP 7.0 chlordiazepoksyd oznaczamy miareczkując 0,1 mol/l r. AgNO3 PK potencjometrycznie.
41

Leki OUN – neuroleptyki, LPD, anksjolityki
Leki Anksjolityczne - inne
7.6 Pochodne difenylometanu
Hydroxyzyny chlorowodorekHydroxizni hydrochloridum EP 7.0(Hydroxizinum VP 10 mg, 25 mg, ATARAX , UBC Pharma)
Hydroxyzyna ma wyraźne działanie przeciwhistaminowe
Reakcje tożsamościowe:1) tworzy pikrynianyRozpuścić 0,1 g związku w metanolu i rozcieńczyć do 15 ml. Dodać 15 ml nasyconego metanolowego roztworu kwasu pikrynowego. Odstawić na 15 minut, wytrąca się osad pikrynianu. Przesączyć, przekrystalizować z metanolu.Zmierzyć temp. topnienia 189 – 192 °C
42

Leki OUN – neuroleptyki, LPD, anksjolityki
7.6 Pochodne alkanodioli
Meprobamat Meprobamatumdwukarbaminian 2-metylo-2-propylopropanodioluFP IV, EP 6.0
Obecnie nie stosowany – powoduje bardzo szybkie uzależnienie.
Reakcje tożsamościowe:1) hydroliza zasadowa w 15% NaOH, po ogrzaniu – wydziela się amoniak2) z odczynnikiem Nesslera (K2HgI4 ) - zabarwienie szare do czarnego3) Reakcja z azotanem kobaltu Rozpuścić 0,2 g substancji w 15 ml 0,5 mol/l metanolowym KOH, i ogrzewać pod chłodnicą zwrotną przez 15 minut.Dodać 0,5 ml kwasu octowego lodowatego, i 1 ml metanolowego roztworu 50g/l Co(NO3).Powstaje ciemnoniebieskie zabarwienie.
43

Leki OUN – neuroleptyki, LPD, anksjolityki
SCHEMAT ANALIZY ZASAD HETEROCYKLICZNYCH i ICH SOLIPierwiastki: azot (N) (+), siarka (S) (+)
poch. fenotiazyny, tioksantenuPierwiastki: azot (N) (+), siarka (S) (-)
poch. dibenzoazepiny, 1,4-benzodiazepiny, butyroferonu
Rozpuszczalność w H2OTAK – sole zasad │NIE – wolne zasady
Sole zasad
1. Rozpuszczalne w H2O nast. dodać 0,5mol/l NaOH - wypada biały osad odpowiedniej wolnej zasady
1a. czasami zamiast osadu oleiste krople, wtedy ekstrakcja eterem, odparować i zbadać pozostałość
2. Reakcje na anion, najczęściej Cl-, inne: SO42- ,winiany
3. reakcja z stęż H2SO4 – zabarwienie czerwone, różna intensywność i odcień – poch. fenotiazyny, tioksantenu
4. reakcja z r. FeCl3 – zabarwienie czerwone – poch. fenotiazyny, tioksantenu
5.Reakcja diazowania i sprzęgania z β-naftolem – wykluczenie sulfonamidów
6. reakcja z kwasem pikrynowym (nasycony roztwór w wodzie) – sole, pikryniany - wyizolować, zmierzyć temp topnienia
Zasady Heterocykliczne
1. Rozpuszczalne w metanolu i rozcieńczonych kwasach
2. Rozpuszczalne w 10% HCl, nast.dodać 0,5mol/l NaOH - wypada biały osad odpowiedniej wolnej zasady
3. reakcja z stęż H2SO4 – zabarwienie czerwone, niebieskie – poch. dibenzoazepiny (Imipramina)- poch. 1,4-benzodiazepiny – żółta fluorescencja (360 nm)- poch. butyroferonu – brak reakcji
4. inne reakcje: H2SO4 /formaldehyd, odcz. Mandelina, Marquisa-Mianseryna - z odcz. Mandelina – zabarwienie fioletowekarbamazepina (Amizepin)
5. reakcja z kwasem pikrynowym – sole, pikryniany - wyizolować, zmierzyć temp topnienia jeżeli podano*)sole zasad nierozpuszczalne w wodzie wykonujemy z metanolowym roztworem kwasu pikrynowego
6. Inne reakcje szczegółowe- 1,3-dinitrobenzenem – poch. butyrofenonu (Haloperidol i inne) i niektóre poch. 1,4-benzodiazepiny
- hydroliza kwaśna do benzofenonu (pochodne 1,4-benzodiazepiny)
- sole z heteropolikwasami
Sprawdzić temp. Topnienia
chromatografia TLC (wykonać badanie jak podano w odpowiedniej monografii)
44

Leki OUN – neuroleptyki, LPD, anksjolityki
45

Leki OUN – neuroleptyki, LPD, anksjolityki
Sole zasad Zasady heterocykliczne
Pochodne fenotiazynyPromazyna, Promazini Hydrochloridum PROMAZINProchlorperazyny maleinianProchlorperazini Maleas,CHLORPERAZINUMPerfenazyna, PerphenazinumFlufenazyna, Fluphenazini dihydrochloridum, Fluphenazini decanoas
Chlorpromazyna, Chlorpromazini HydrochloridumFENACTIL (Polfa, Warszawa)Trifluoperazyna, Trifluoperazini HydrochloridumSTELAZINE (GlaxoSmithKline)Tiorydazyna, Thioridazinum THIORIDAZINE Levomeproazyny maleinian, Levomepromazini Maleas,(TISERCIN)
Pochodne fenotiazyny o działaniu przeciwwymiotnymTietylperazyna, Thiethylperazine maleate (TORECAN, Krka, Novartis) USP 24Nie farmakopeaneTioperazyna, Thioproperazine (MAJEPTYL, Sanofi-Aventis )Metopimazyna, Metopimazine, (VOGALEN, Schwarz Pharma; Sanofi-Aventis )
Pochodne butyrofenonuHaloperydol Haloperidolum
Haloperydolu dekanonian, Haloperidoli decanoas
Bromperydol,Bromperidolum
Bromperydolu dekanonian, Bromperidoli decanoas
Benperydol,Benperidolumm.cz. 381,4
Droperydol,Droperidolumm.cz. 379,4
Pochodne tioksantenuChlorprotyksen, Chlorprotixeni Hydrochloridum,(TARACTAN )Klopentyksol, Zuklopentyksolu dekanonian,Zuclopenthixoli decanoas, (CLOPIXOL)Flupentyksol, Flupentixoli dihydrochloridum,
pochodna difenylobutylopiperydynyFluspirylenFluspirylenumIMAP (Janssen Pharm.),
pochodna dibenzo[b,e]-1,4-diazepinyKlozapina
46

Leki OUN – neuroleptyki, LPD, anksjolityki
Sole zasad Zasady heterocykliczne
(FLUANXOL)Pochodne benzamidu
SulpirydSulpirydumSULPIRYD (Pliva -Kraków)
ClozapinumLEPONEX (Novartis Pharma)KLOZAPOL (Egis Pharm. PLC)
pochodne 1,4-benzodiazepiny
Chlordiazepoksydu chlorowodorekChlordiazepoxidi chydrochlorodum,ELENIUMDiazepamDiazepamum,RELANIUM OxazepamOxazepamum, KlonazepamClonazepamum,NitrazepamNitrazepamumFlunitrazepamFlunitrazepamum,ROHYPNOL (Glaxo)AlprazolamAlprazolamum XANAX
TriazolamUSP 24
47

Leki OUN – neuroleptyki, LPD, anksjolityki
Debian GNU/Linux
Libreoffice.org
Widma IR zostały wykonane w Zakładzie Chemii Organicznej Uniwersytetu Medycznego w ŁodziSpektrometr FTIR Infinity Series firmy ATI Mattson.
48
![Catálogo Kubota Miniexcavadora U20-3aS · 0itxlqdv srolydohqwhv \ px\ yhuviwlohv txh jdudqwl]dq xq dowr uhqglplhqwr \ pi[lpd vhjxulgdg 6lvwhpd gh wudvodflyq-pt ufssfopt bddjefoubept](https://static.fdocuments.pl/doc/165x107/5f3e38b61352cd77d1050567/catlogo-kubota-miniexcavadora-u20-3as-0itxlqdv-srolydohqwhv-px-yhuviwlohv-txh.jpg)