H2OBŁĘDNI w laboratorium chemicznym UAM
description
Transcript of H2OBŁĘDNI w laboratorium chemicznym UAM

H2OBŁĘDNI w laboratorium chemicznym UAM

Elektroliza wodyOpis eksperymentuKapilarna pipetę Pasteura wypełniamy w ¾ pojemności roztworem wodorotlenku
sodu. Banieczkę pipety przebijamy na wylot dwiema szpilkami (szpilki nie mogą się stykać). Do każdej ze szpilek podłączamy przewody z krokodylkami. Wolne końce przewodów przyłączamy do baterii. Wylot pipety zanurzamy w wodzie z płynem do mycia naczyń umieszczonej na szalce Petriego. Wydzielający się gaz zbieramy w bańkach mydlanych. Kiedy baniek mydlanych będzie ? rozłączamy cały układ. Po chwili zbliżamy zapaloną wykałaczkę.
ObserwacjeNa elektrodach wydziela się bezbarwny gaz.Gaz w pęcherzykach spala się wybuchowo.
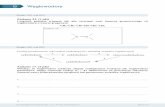
WnioskiPod wpływem prądu woda ulega elektrolizie, czyli rozkłada się na wodór i tlen.
2H₂O 2H₂ + O₂
Wodór spala się w tlenie wybuchowo (tworzą tzw. Mieszaninę piorunującą).2H₂ + O₂ 2H₂O


Odwodnienie cukru
Opis eksperymentuDo wąskiej zlewki o pojemności 150 cm³ sypiemy cukier (ok. 1-2 wysokości), można
zwilżyć jego powierzchnię paroma kroplami wody, a następnie nalewamy ok. 20 cm³ stężonego kwasu siarkowego (VI). Obserwujemy zmianę zabarwienia cukru, sprawdzamy temperaturę zlewki.
ObserwacjeZawartość zlewki zmienia barwę z białej na czarną i zwiększa swą objętość.
WnioskiPod wpływem stężonego H₂SO₄ sacharoza ulega odwodnieniu, co prowadzi do
zwęglenia cukru.



Woda utleniona a pasta dla słonia
Opis eksperymentuDo szklanego cylindra obj. 250 ml, ustawionego w misce lub kuwecie, wlewamy 30 ml
perhydrolu i niewielką ilość płynu do mycia naczyń, mieszamy. Jednym, śmiałym ruchem wlewamy do cylindra 5 ml stężonego roztworu jodku potasu.
ObserwacjeZawartość cylindra pieni się i zwiększa swoją objętość, wypływając poza naczynie.
WnioskiNadtlenek wodoru rozkłada się z wydzieleniem tlenu, który pod wpływem płynu do
mycia naczyń tworzy pianę.



Otrzymywanie wodorotlenku sodu
Opis eksperymentuUstawiamy mały krystalizator lub szalkę Petriego na płycie grafoskopu. Do naczynia
wlewamy około 5 cm³ wody. Do wody dodajemy 2-3 krople roztworu fenoloftaleiny. Wyjmujemy z pojemnika kawałek sodu (który przechowuje się pod naftą), osuszamy go bibułą filtracyjną i nożem odcinamy kawałeczek metalu. Wrzucamy sód do naczynia z wodą i na ekranie obserwujemy przebieg doświadczenia.
ObserwacjeSód rozpuszcza się w wodzie. Wydziela się gaz. Fenoloftaleina barwi się na malinowo.
WnioskiSód reaguje energicznie z wodą.
2Na + 2H₂O 2NaOH + H₂


Rozkład nadtlenku wodoru z udziałem katalizatora
Opis eksperymentuDo trzech probówek nalewamy roztwór nadtlenku wodoru. Następnie do pierwszej
probówki wrzucamy niewielką ilość tlenku manganianu(IV), do drugiej grudkę drożdży, do trzeciej KMnO₄. Identyfikujemy gazy wydzielające się w probówkach.
ObserwacjePo dodaniu MnO₄, drożdży i KMnO₄ energicznie wydzielał się gaz, który powodował
zapalenie się żarzącego się łuczywka.
WnioskiPod wpływem katalizatorów nadtlenek wodoru rozkłada się z wydzieleniem tlenu.
2H₂O₂ 2H₂O + O₂
kat.


Reakcja tlenku węgla(IV) z zasadą wapniową
Opis eksperymentuDo probówki nalewamy około 2 cm³ wody wapiennej, czyli roztworu wodorotlenku
wapnia (zasady wapniowej), a następnie wkładamy do niego rurkę szklaną i wdmuchujemy przez nią powietrze wydychane z płuc.
ObserwacjeWoda wapienna mętnieje.
WnioskiWodorotlenek wapnia reaguje z CO₂, tworząc nierozpuszczalny w wodzie CaCO₃.
Ca(OH)₂ + CO₂ CaCO₃ + H₂O


Fontanna z wody amoniakalnej
Opis eksperymentuW kolbie okrągło dennej ogrzewamy wodę amoniakalną. Wydzielający się gaz
zbieramy w odwróconej do góry dnem kolbie (amoniak jest gazem lżejszym od powietrza). Kolbę z zebranym gazem zamykamy korkiem z osadzoną w nim rurką szklaną zakończoną wężykiem gumowym ze ściskaczem. Koniec wężyka gumowego zanurzamy w zlewce pojemności 1000 cm³ z wodnym roztworem fenoloftaleiny, po czym zwalniamy ściskacz i obserwujemy co dzieje się we wnętrzu kolby oraz jakie zachodzą zmiany.
ObserwacjeDo wnętrza kolby zostaje zassana woda. Wskaźnik (wywar z czerwonej kapusty)
zmienia zabarwienie z fioletowego na zielony.
WniosekAmoniak bardzo dobrze rozpuszcza się w wodzie (około 720 objętości w 1 objętości
wody). Woda amoniakalna ma odczyn zasadowy.


Działanie wody bromowej na olej roślinny i smalec
Opis eksperymentuW probówkach umieszczamy niewielką ilość (ok. 0,5 – 1cm³) oleju roślinnego i smalcu
doprowadzonego do postaci płynnej przez lekkie ogrzanie probówki, np. w ciepłej wodzie. Do obu probówek dodajemy po 1 cm³ wody bromowej bądź przygotowanego ,,In situ” roztworu bromu. Zamykamy probówki korkiem i intensywnie mieszamy. Obserwujemy zawartość probówek.
ObserwacjePo wymieszaniu woda bromowa odbarwiła się w probówce z olejem roślinnym. W
probówce ze smalcem woda bromowa nie odbarwiła się.
Wnioski
RCH = CHR’ + Br₂ RCHBrCHBrR’
Woda bromowa pozwala odróżnić tłuszcze nienasycone od nasyconych.






![Współczesne Tendencje Przekładoznawcze [Wydawnictwo Naukowe UAM]](https://static.fdocuments.pl/doc/165x107/56d6c0621a28ab30169a2bcc/wspolczesne-tendencje-przekladoznawcze-wydawnictwo-naukowe-uam.jpg)