Prezentacja programu PowerPoint...Prezentacja programu PowerPoint Author Tomasz Lubera Created Date...
Transcript of Prezentacja programu PowerPoint...Prezentacja programu PowerPoint Author Tomasz Lubera Created Date...

Tomasz Lubera

Zadanie 1
•Zadanie:
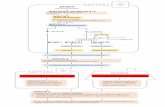
•Entropia ciekłego etanolu w temperaturze 298 K jest równa 160,7 JK-1mol-1. Ciśnienie par etanolu w tej temperaturze wynosi 59 mmHg. Ciepło parowania etanolu w temperaturze 298 K wynosi 42,6 kJmol-1. Oblicz entropię jednego mola par etanolu pod ciśnieniem 9500 Pa w temperaturze 313 K. Molowa pojemność cieplna par etanolu wynosi 145 JK-1mol-1.
•Odpowiedź:
•𝑆313 = 309,2 J ∙ K−1
Ćwiczenia rachunkowe z chemii fizycznej - Druga i Trzecia Zasada Termodynamiki - Zadania 2

Zadanie 2 • Zadanie: Oblicz zmianę entropii reakcji: 2Al + 3/2O2 =
Al2O3 w temperaturze 1100 K pod ciśnieniem 1013 hPa.
•Odpowiedź: ∆𝑆1100 = −332,609 J ∙ K−1
Ćwiczenia rachunkowe z chemii fizycznej - Druga i Trzecia Zasada Termodynamiki - Zadania 3
Izobaryczne molowe pojemności cieplne 𝐶𝑝 = 𝑎 + 𝑏𝑇 + 𝑐𝑇2 + 𝑑𝑇−2 J ∙ mol−1 ∙ K−1
Substancja a b /∙10-3/ c /∙10-6/ d /∙105/ Zakres temperatur, K O2(g) 25,76 12,997 -3,867 298-3000 Al(s) 20,112 13,911 298-933 Al(c) 29,33 933-2733
Al2O3(s) 103,074 25,14 -29,33 298-1700
Ciepła przemian fazowych oraz wartości funkcji termodynamicznych w warunkach standardowych
Substancja Ttopnienia
K
Ciepło topnienia J∙mol-1
Twrzenia K
Ciepło parowania J∙mol-1
Entropia standardowa J∙mol-1∙K-1
Al 933 10475,0 2723 291205 28,366 O2 54,2 444,1 90 6829,2 205,394
Al2O3 2293 108940,0 - - 52,375

Zadanie 3
•Zadanie:
•Po ogrzaniu 4 dm3 argonu pod stałym ciśnieniem 2,026∙105 Pa objętość gazu wzrosła do 12 dm3. Temperatura początkowa wynosiła 320 K. Oblicz zmianę entropii przy założeniu, że argon zachowuje się jak gaz doskonały.
•Odpowiedź:
•ΔS320 = 6,956 J∙K-1
Ćwiczenia rachunkowe z chemii fizycznej - Druga i Trzecia Zasada Termodynamiki - Zadania 4

Zadanie 4
•Zadanie:
•Oblicz jakiej objętości końcowej odpowiada zmiana entropii równa 38,28 J∙K-1 jeżeli jeden mol gazu doskonałego zajmujący w warunkach początkowych objętość 0,02 m3 ulega izotermicznej ekspansji.
•Odpowiedź:
•v2 = 2 m3
Ćwiczenia rachunkowe z chemii fizycznej - Druga i Trzecia Zasada Termodynamiki - Zadania 5

Zadanie 5
•Zadanie:
•Oblicz zmianę entropii związana z ogrzewaniem 40 g helu (traktowanego jako gaz doskonały) od 270 K do 400 K:
• w stałej objętości,
• przy stałym ciśnieniu.
•Odpowiedź:
•ΔSv = 49,02 J∙K-1
•ΔSp = 81,69 J∙K-1
Ćwiczenia rachunkowe z chemii fizycznej - Druga i Trzecia Zasada Termodynamiki - Zadania 6

Zadanie 6
•Zadanie:
•Oblicz ΔU, ΔH, ΔS, ΔF i ΔG gdy 90 g wody przechodzi w parę w temperaturze 373 K i pod ciśnieniem 10328,746 mmH2O. Objętość molowa wody ciekłej wynosi 18 cm3 zaś objętość molowa pary wynosi 30,6 dm3, ciepło parowania wody wynosi 9,82 kcal∙mol-1.
•Odpowiedź:
•ΔU = 190,01∙103 J ΔF = -15,49∙103 J
•ΔH = 205,50∙103 J ΔG = 0 J
•ΔS = 550,94 J∙K-1
Ćwiczenia rachunkowe z chemii fizycznej - Druga i Trzecia Zasada Termodynamiki - Zadania 7

Zadanie 7
•Zadanie: •Oblicz ΔS i ΔG procesu krzepnięcia jednego mola MnO
przechłodzonego do temperatury 2000 K pod stałym ciśnieniem 1 atm. Molowe pojemności cieplne ciekłego i stałego MnO wynoszą odpowiednio 50,9 J∙K-1∙mol-1 i 60,294 + 6,788∙10-3T J∙K-1∙mol-1. Temperatura topnienia wynosi 2058 K zaś ciepło topnienia w tej temperaturze 54470 J∙mol-1.
•Odpowiedź: •ΔG = -1553,62 J
•ΔS = -27,13 J∙K-1
Ćwiczenia rachunkowe z chemii fizycznej - Druga i Trzecia Zasada Termodynamiki - Zadania 8